
缺氧诱导因子(HIF):生命与疾病的"双刃剑"
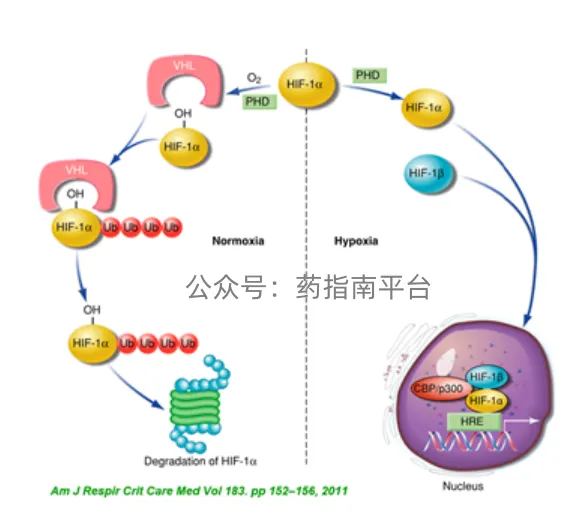
2019年诺贝尔生理学或医学奖授予了威廉·凯林(William G. Kaelin Jr)、彼得·拉特克利夫(Sir Peter J. Ratcliffe)和格雷格·塞门扎(Gregg L. Semenza),以表彰他们发现细胞感知和适应氧气变化的机制——缺氧诱导因子(HIF)。
这一机制本是生命进化的杰作:当细胞缺氧时,HIF会激活血管生成、红细胞增殖等通路,帮助机体存活。然而在VHL病和肾癌中,HIF-2α的异常累积却成了"癌症引擎"——驱动肿瘤血管疯狂生长,甚至引发全身多器官病变。
贝组替凡:精准狙击HIF-2α的"分子导弹"
贝组替凡的研发正是基于这一发现。作为全球首个HIF-2α抑制剂,它通过特异性结合HIF-2α蛋白,阻断其与DNA的结合,从而精准抑制下游致癌信号(如VEGF、EPO等)。这种"靶向爆破"不仅疗效显著,更因口服给药极大提升了治疗便捷性。
VHL病:全身多器官的"定时炸弹"
VHL病是一种常染色体显性遗传病,患者因VHL基因突变导致HIF-2α异常累积,60%-70%会发展为肾细胞癌,70%出现中枢神经系统血管母细胞瘤,10%-17%罹患胰腺神经内分泌肿瘤。传统治疗依赖反复手术切除,但器官损伤和复发风险极高。
关键数据:LITESPARK-004研究震撼发布
2021年《新英格兰医学杂志》发表的Ⅱ期临床试验显示:
61例VHL相关肾细胞癌患者接受贝组替凡治疗,客观缓解率(ORR)达49%(RECIST标准),远超历史对照(手术切除后5年复发率>80%);
中位治疗时间21.8个月,89%患者肿瘤体积持续缩小;
中枢神经系统血管母细胞瘤和胰腺神经内分泌肿瘤的缓解率分别为63%和83%;
3级及以上不良反应发生率仅6%,以贫血最常见且可控。
案例故事
32岁程序员张先生,VHL基因突变携带者,5年内经历3次肾癌手术、1次脑肿瘤切除。2022年接受贝组替凡治疗后,肾脏肿瘤体积缩小42%,胰腺病灶完全消失,目前持续治疗中,生活质量显著改善。
晚期肾癌:耐药后的至暗时刻
即使PD-1/PD-L1抑制剂联合VEGF-TKI一线治疗有效率可达60%,但约50%患者在1年内进展,后线治疗选择匮乏,中位生存期不足12个月。
破冰数据:LITESPARK-005研究改写指南
2023年ASCO年会公布的Ⅲ期研究显示,针对既往接受过PD-1/L1抑制剂和VEGF-TKI治疗的晚期肾癌患者:
贝组替凡组中位无进展生存期(PFS)5.6个月,显著优于对照组(依维莫司)的3.9个月(HR=0.70);
客观缓解率(ORR)22% vs 4%,完全缓解(CR)率3%;
在肉瘤样分化(预后极差亚型)患者中,PFS优势更明显(5.3个月 vs 2.8个月)。
贝组替凡的独特机制使其对传统治疗耐药肿瘤仍有效,且对侵袭性亚型有特殊优势,为晚期患者提供了"续命"关键选择。

价格&规格
40mg/片,90片/盒。¥7900
适用人群
VHL病相关肾癌/CNS血管母细胞瘤/pNET(无需立即手术)
晚期肾癌(既往接受过PD-1/L1抑制剂+VEGF-TKI治疗)
用药方案
每日一次口服120mg,空腹或随餐服用,需持续至疾病进展或不可耐受毒性。
副作用管理
贫血(发生率90%,3级及以上占7%):可通过促红细胞生成素(EPO)治疗
疲劳(32%)、头痛(20%):对症支持即可缓解
禁忌症
妊娠期禁用(可能致胎儿畸形),用药期间需严格避孕。
从诺奖实验室到患者床头,贝组替凡的诞生完美诠释了"转化医学"的真谛——它不仅让VHL病患者摆脱了终身手术的噩梦,更为晚期肾癌耐药患者点燃了希望之火。正如威廉·凯林教授所言:"我们不是在对抗疾病,而是在解码生命的语言。"而这把钥匙,正在打开更多癌症治疗的大门。
<<< END >>>
公众号内免费资源:
1.《梅奥诊所乳腺癌抗癌权威指南》——回复“梅奥乳腺癌”
2.《类风湿关节炎患者教育与就医指南》——回复“类风湿关节炎”