
非小细胞肺癌(NSCLC)患者中 ALK 基因突变的比例约为 3% 至 5%。在 NSCLC 的各类致癌驱动基因变异里,ALK 融合 / 重排乃是继 EGFR 之后的第二大常见突变,其发生率处于 3% 至 7% 之间。尽管 ALK 突变的发生概率并不高,然而 ALK 抑制剂对这类患者呈现出较高的治疗响应率,患者 5 年生存率超过 60%,故而 ALK 突变被誉为 “钻石突变”。迄今为止,已有多种 ALK 抑制剂在全球范围内获得批准,用于治疗携带 ALK 突变的 NSCLC 患者。
目前,在接受第一 / 二代 ALK 酪氨酸激酶抑制剂(TKI)治疗后,大约 50% 的患者会出现耐药性突变。对于那些已经接受过两种或更多 ALK TKI 治疗的患者,当下的治疗指南尚未给出明确的治疗标准。
已获批上市的一二三代ALK靶向药

2024 年 5 月 16 日,Nuvalen 公司宣称,美国食品药品监督管理局(FDA)将突破性疗法认定(BTD)授予了 NVL-655,该认定适用于治疗局部晚期或转移性 ALK 阳性非小细胞肺癌(NSCLC)患者,这些患者此前曾接受过两种或多种 ALK 酪氨酸激酶抑制剂(TKI)的治疗。这一认定是基于 NVL-655 在治疗晚期 ALK 阳性 NSCLC 患者方面所展现出的潜力,特别是在那些对现有治疗已经产生耐药性的患者当中。

NVL-655 属于第四代 ALK-TKI(酪氨酸激酶抑制剂)。它兼具抗 ALK 活性、良好的脑渗透性,同时可避免 TRK 相关的神经毒性,旨在应对第三代 ALK-TKI 产生的耐药问题。体外研究表明,NVL-655 对 ALK 融合及其耐药突变有着强效的抑制作用。目前,NVL-655 在针对 ALK 耐药非小细胞肺癌(NSCLC)患者的 I 期试验中已取得积极数据。在安全性方面,NVL-655 表现出良好的耐受性,治疗相关不良事件较为轻微。
ALKOVE-1 研究(NCT05384626)是一项包含两个阶段的临床试验,分别为 I 期剂量递增阶段与 II 期扩展阶段。该研究的 II 期扩展阶段会依据肿瘤类型以及患者既往接受的治疗情况进行分组。I 期研究的主要目标在于确定 NVL-655 在 II 期研究中的推荐剂量,同时明确该药物的最大耐受剂量。这将为后续的研究提供关键的剂量选择依据,用以评估 NVL-655 在治疗 ALK 阳性非小细胞肺癌(NSCLC)患者时的疗效与安全性。

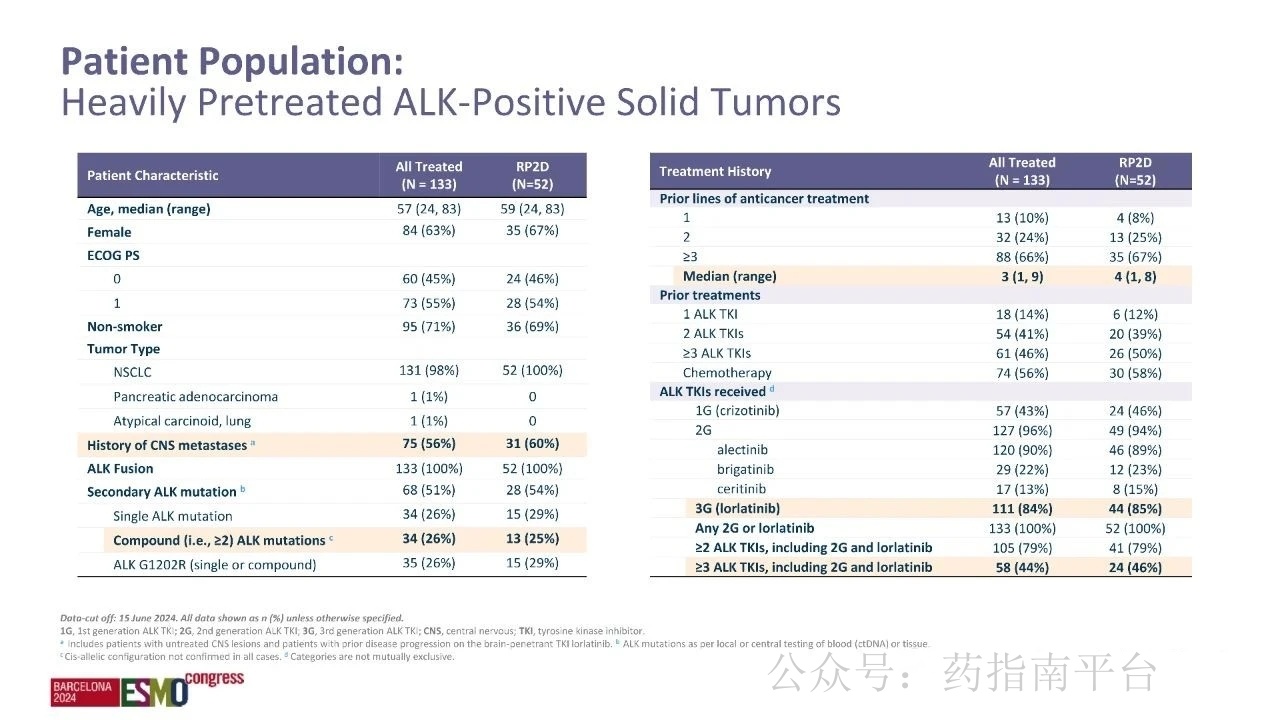
截至 2024 年 6 月 15 日,该研究的 1 期部分共招募了 133 名患者,其中 103 名患者进行了疗效评估。研究中患者接受的剂量范围为每天 15 毫克至 200 毫克,尚未达到最大耐受剂量。综合各种因素,将 150 毫克每日剂量选定为推荐的 2 期剂量(RP2D),包括扩展队列在内,有 52 例患者接受了 RP2D 治疗。
在 RP2D 剂量组中,患者的中位年龄为 59 岁,其中三分之二为女性(占比 67%)。体能状态为 0 的患者占 46%,为 1 的占 54%。大多数患者为非吸烟者(占比 69%)。超过一半的患者(60%)在基线时有脑转移史,且均存在 ALK 融合,继发性 ALK 突变为单一突变或 ALKG1202R 突变。既往治疗的中位数为 4 次(范围为 1 至 8 次),一半(50%)的患者既往接受过 3 次或更多次的 ALK 酪氨酸激酶抑制剂(TKI)治疗,所有患者均接受过第二代或更优的 TKI。58% 的患者既往接受过化疗。最常见的既往 TKI 为第二代药物(占比 94%),85% 的患者还接受了劳拉替尼治疗。
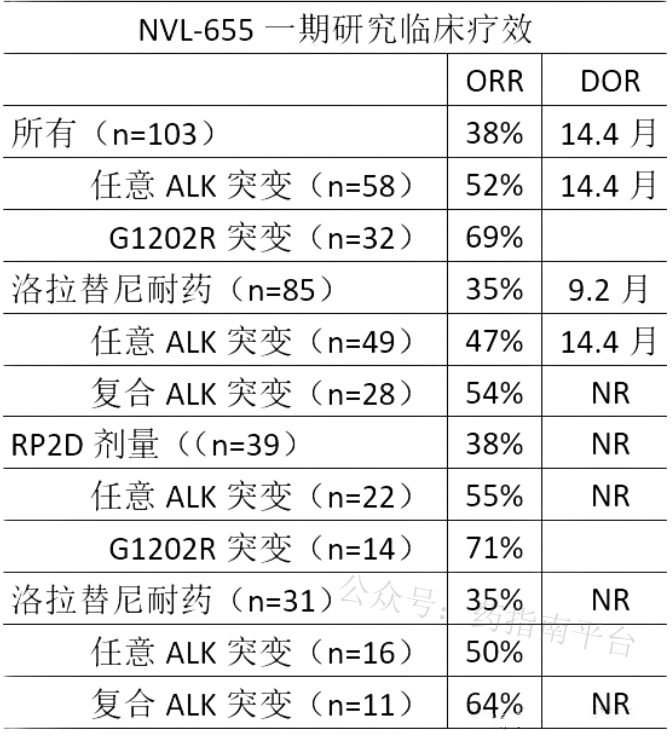
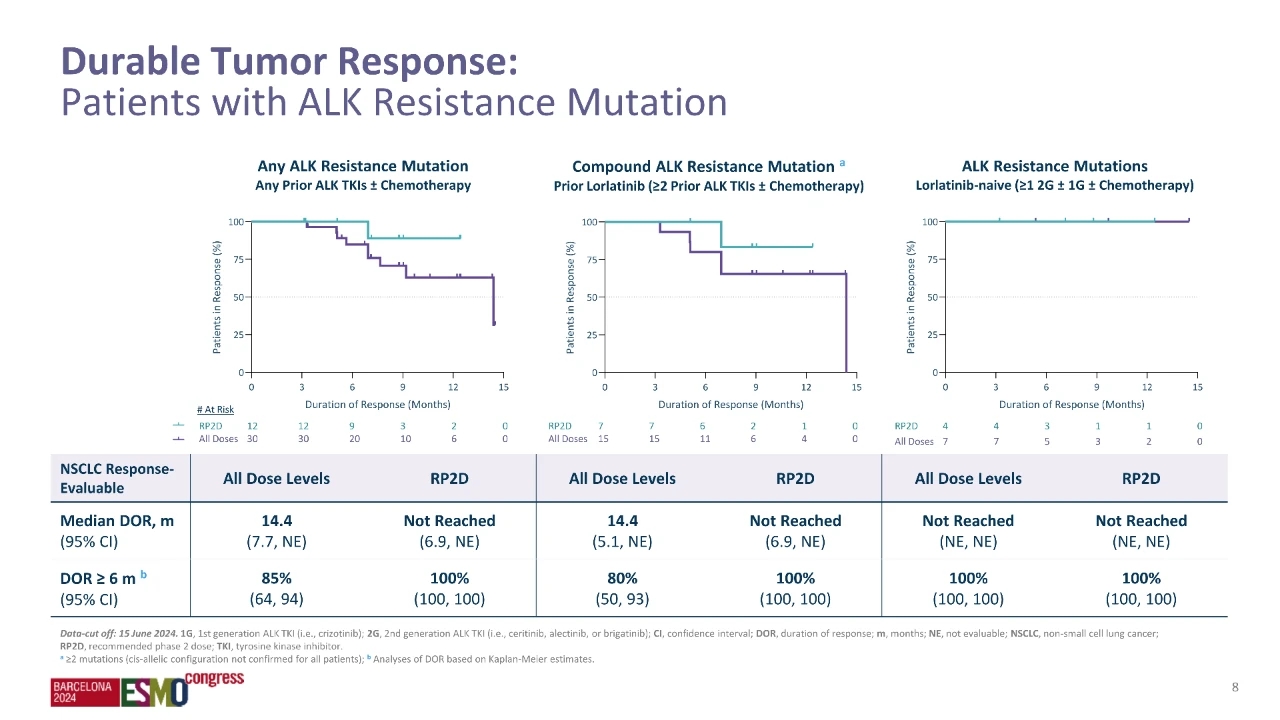
在所有剂量组中,有 103 例患者可供评估,其客观有效率(ORR)为 38%,中位缓解持续时间(DOR)为 14.4 个月。在推荐的 2 期剂量(RP2D)组,有 39 例患者可供评估,客观有效率同样为 38%,中位缓解持续时间尚未成熟(NR),且半年以上的比例为 100%。
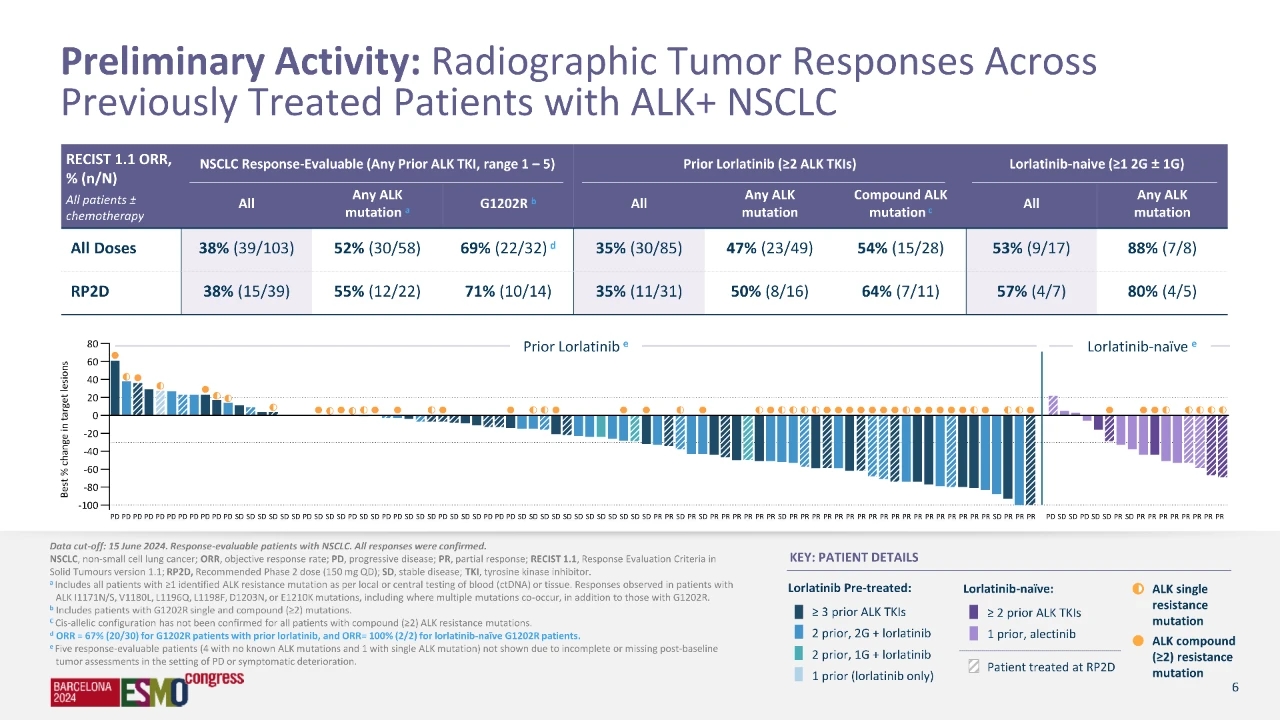
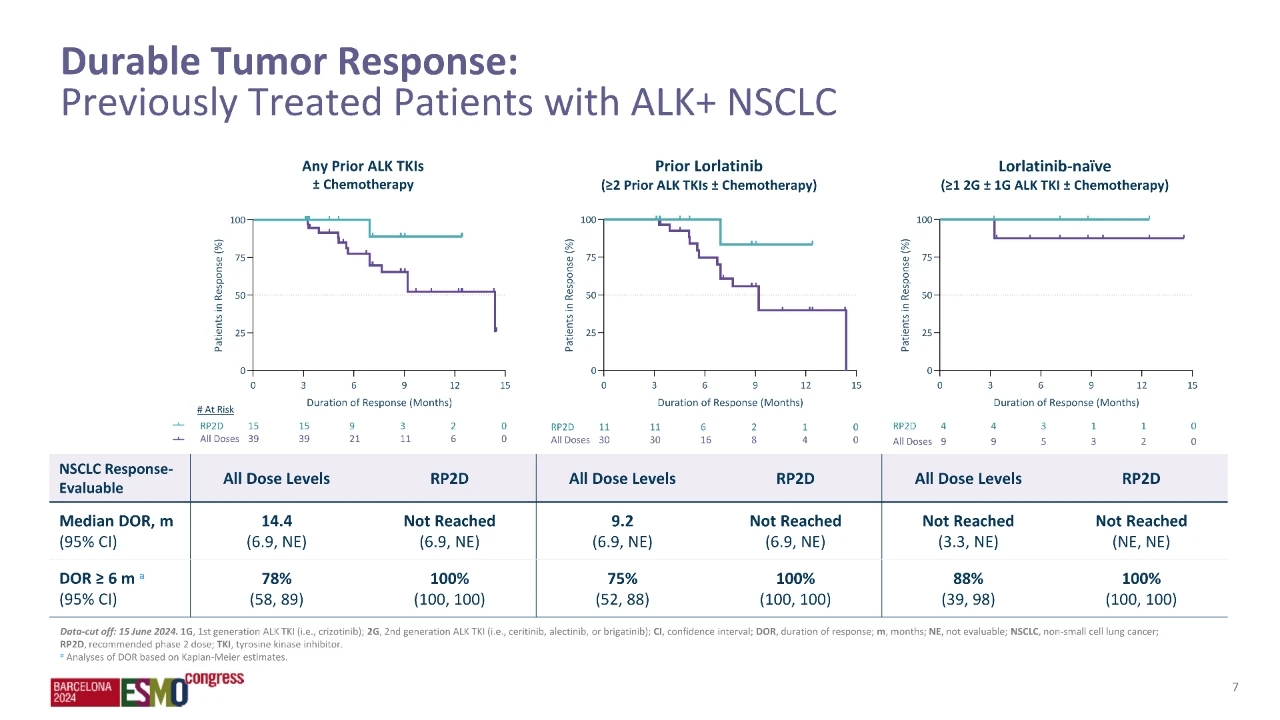
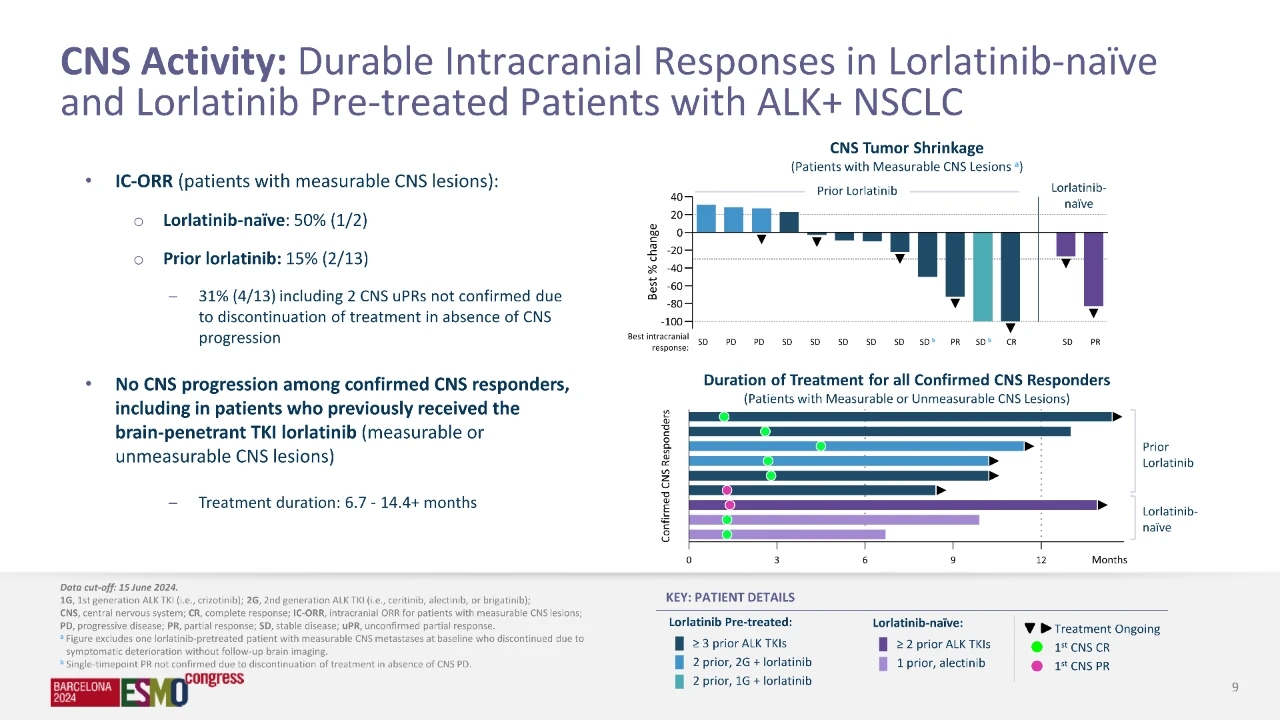
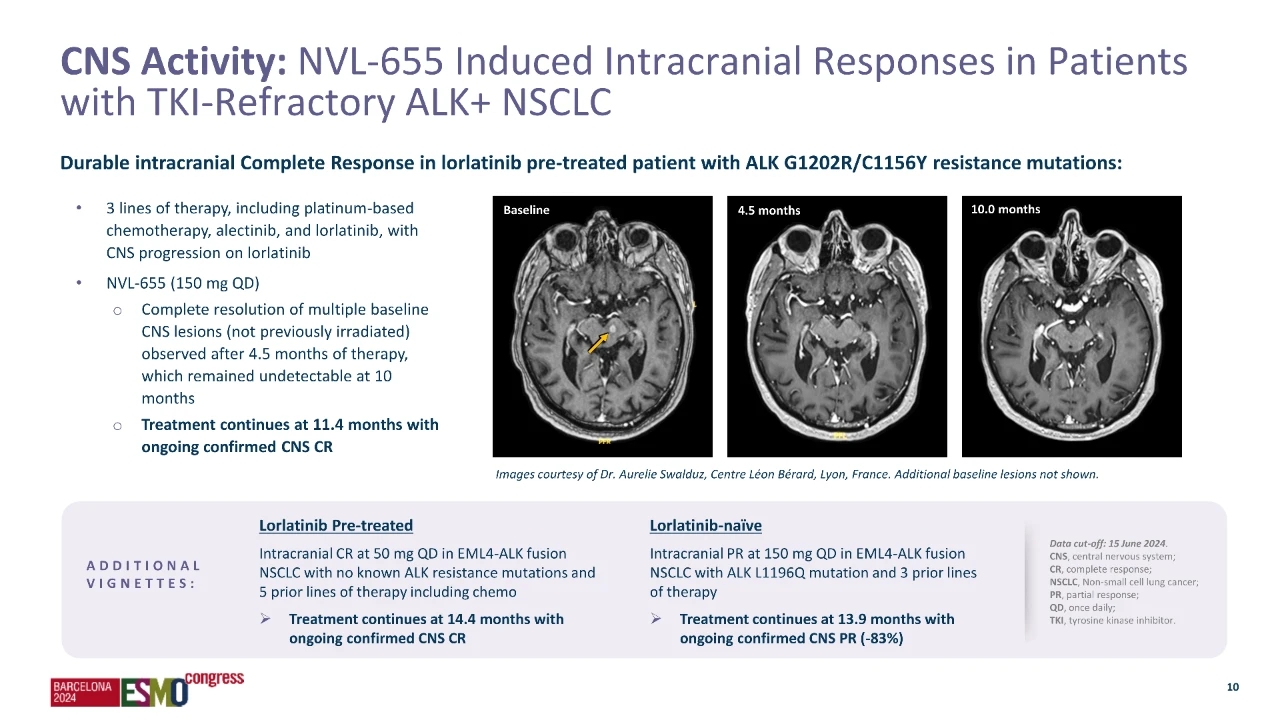
颅内客观缓解率(ORR)在未接受过劳拉替尼的患者中为 50%(1/2),在既往接受过劳拉替尼的患者中为 15%(2/13)。此外,在确诊有中枢神经病变的患者中,31%(13 例中有 4 例)有未经证实的颅内 ORR,但在随访前因无中枢神经活动而停止治疗。在确诊的中枢神经反应者中未观察到病情进展,包括之前接受过较低剂量劳拉替尼治疗的患者。
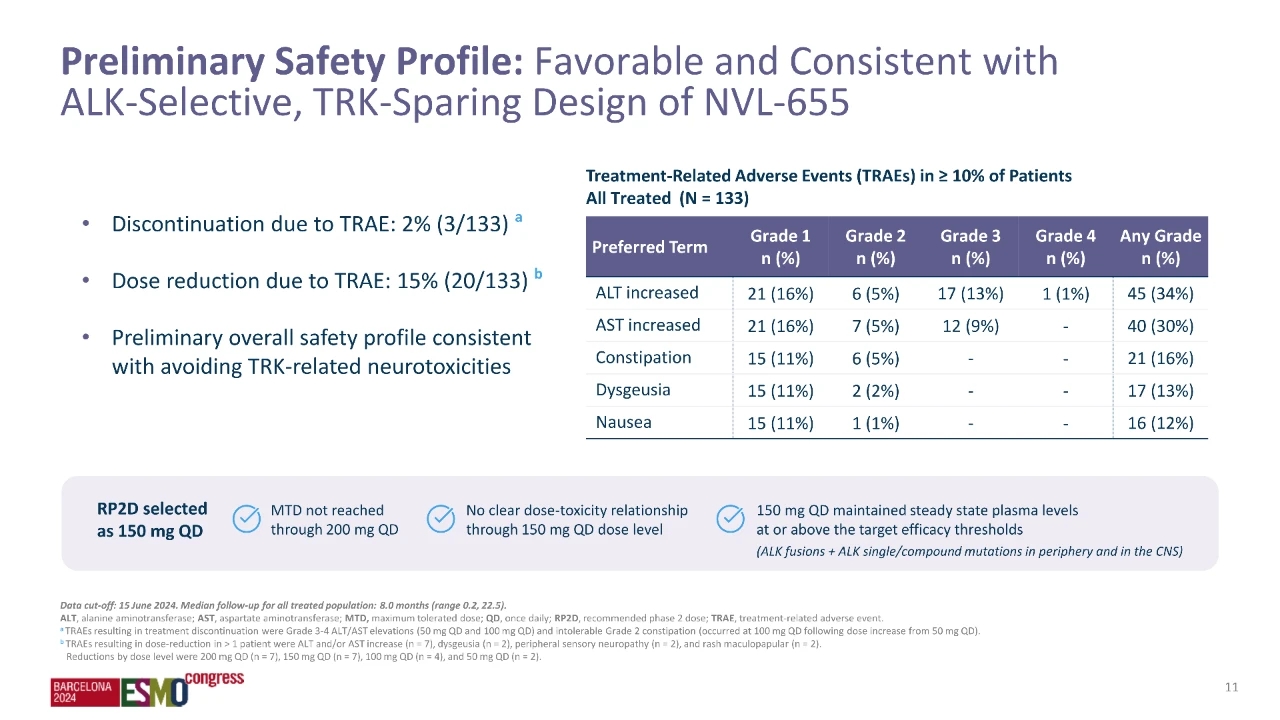
133 例患者可用于评估 NVL-655 的安全性。在所有剂量水平上,大多数治疗相关不良事件的严重程度为 1 级和 2 级。NVL-655 导致的停药率为 2%,15% 的患者需要减少剂量。其中最常见的不良事件是 ALT(丙氨酸氨基转移酶)升高(占比 34%)和 AST(天冬氨酸氨基转移酶)升高(占比 30%)。13% 的患者出现 3 级 AST 升高,其中 1 名患者出现 4 级事件;9% 的患者出现 3 级 ALT 升高,无 4 级事件。其他常见的不良事件严重程度均为 1 级和 2 级,最常见的包括便秘(占比 16%)、消化不良(占比 13%)和恶心(占比 12%)。


在 ALKOVE-1 研究的试验中,NVL-655 对经过多线治疗后的晚期 ALK 阳性非小细胞肺癌(NSCLC)患者展现出了良好的疗效与安全性。药动学和药效学数据支撑了其对耐药突变的覆盖作用,并且该药物具有良好的耐受性,常见不良事件较为轻微且易于控制。